随着纳米技术与生物医学的深度融合,开发高效、精准的药物递送系统已成为现代药学的前沿课题。其中,将先进纳米材料与天然活性成分结合,构建智能响应型递送平台,为中药的现代化和精准化治疗带来了革命性机遇。一种基于三磷酸腺苷(ATP)响应的新型组装体——量子点(QD)-酚醛纳米团簇(NC)系统,展现出将纳米药物靶向递送至病变部位的巨大潜力,为中药活性成分的成药性提升开辟了新路径。
一、 核心技术:QD-NC组装体的构建与特性
量子点(QD)作为一种半导体纳米晶体,具有优异的光学特性,如尺寸可调的荧光发射、高亮度与光稳定性,使其成为理想的生物成像与示踪探针。酚醛纳米团簇(NC)通常由天然多酚(如单宁酸、没食子酸等)与金属离子通过配位作用自组装而成,具有良好的生物相容性、可降解性及丰富的表面官能团,易于进一步功能化。
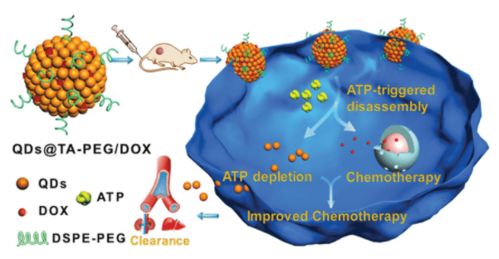
通过精密的界面工程与组装技术,将QD嵌入或共价连接至酚醛NC的网状结构中,可以形成结构稳定的QD-NC杂化纳米组装体。该组装体不仅继承了QD的成像功能,还具备了NC的载药能力、pH响应性以及通过表面修饰实现主动靶向的潜力。
二、 ATP响应机制:实现病灶部位精准释放的关键
三磷酸腺苷(ATP)是细胞内的“能量货币”,其浓度在细胞内外存在巨大差异(细胞内毫摩尔级 vs. 细胞外纳摩尔级)。更重要的是,在肿瘤微环境、炎症部位或缺血/再灌注损伤区域,细胞外ATP浓度会异常升高。这一生物学特性为设计刺激响应型药物递送系统提供了完美靶点。
研究者通过对酚醛NC进行功能化修饰,引入ATP适配体或对ATP敏感的化学键(如磷酸酯键)。当QD-NC组装体在血液循环中运行时,其结构保持稳定,药物被有效封存。一旦抵达ATP浓度异常升高的病变组织,高浓度的ATP会作为“钥匙”,特异性触发组装体的结构解离或孔道开放,从而实现药物的精准、快速释放。这种“智能开关”机制极大地提高了药物的利用度,并最大限度地降低了对正常组织的脱靶毒性。
三、 赋能中药成药:解决溶解度、靶向性与可视化难题
许多中药活性成分(如黄酮类、生物碱、萜类化合物)尽管疗效确切,但普遍面临水溶性差、体内代谢快、缺乏靶向性、生物利用度低等成药性瓶颈。QD-NC-ATP智能递送系统为这些难题提供了系统性解决方案:
- 增溶与保护:疏水性中药成分可以被有效负载于QD-NC组装体的疏水核心或通过π-π堆积、氢键等作用吸附于酚醛网络中,显著提高其水溶性与稳定性,避免在血液循环中被过早降解或清除。
- 主动与被动靶向协同:一方面,纳米尺寸的组装体可通过增强渗透与滞留(EPR)效应被动富集于肿瘤等病变组织;另一方面,可在组装体表面进一步偶联针对病变细胞特定受体的靶向分子(如叶酸、多肽),实现主动靶向。ATP响应机制则确保了药物在靶点处的可控释放。
- 治疗与成像一体化(诊疗一体):QD的荧光特性使得整个递送过程可以被实时、无创地光学成像监控。研究人员可以直观追踪纳米载体在体内的分布、靶向积累情况以及药物释放动力学,实现疗效的实时评估与治疗方案优化,这正符合现代精准医疗的理念。
四、 前景与挑战
将ATP响应的QD-NC组装体应用于中药纳米药物的靶向递送,代表了材料科学、分子生物学与传统药学交叉创新的重要方向。它不仅能提升经典中药方剂或单一活性成分的治疗效能,还有助于阐明其体内作用机理,推动中药走向“量化、可视化、精准化”。
该技术走向临床转化仍面临一些挑战,包括大规模制备的工艺稳定性、组装体长期毒性与免疫原性的全面评估、体内代谢途径的详细解析,以及针对不同中药成分的个性化载体设计等。未来研究需加强跨学科合作,在确保安全性的前提下,优化系统设计,最终开发出具有国际竞争力的中药智能纳米药物。
新型ATP响应性量子点-酚醛纳米团簇组装体,巧妙地利用了疾病微环境的生化特征,构建了一个集靶向递送、智能释药与实时成像于一体的多功能平台。这一前沿技术有望成为破解中药活性成分成药性瓶颈的利器,加速中药现代化进程,为全球患者提供更高效、更安全的治疗方案。